【摘要】目的:对蜂胶的食用安全性进行毒理学实验评价。
方法:采用小鼠急性经口毒性试验、遗传毒性试验(A-mes试验、小鼠骨髓微核试验、小鼠精子畸形试验)和30d喂养试验进行检测评价。
结果:小鼠急性经口毒性MTD>10.0g/kg.bw,三项遗传毒性试验结果均为阴性。30d喂养试验未显示明显毒性。
结论:蜂胶软胶囊急性毒性分级属实际无毒级,无遗传毒性,按推荐量食用是安全的。
【作者】 1 谢玮 1 郭婕 1 卢连华 2 薛薇(1 山东省疾病预防控制中心,山东济南 250014。2 山东大学医学院2007级一班 山东济南 250012)
【关键词】蜂胶 急性毒性 遗传毒性30d喂养试验 安全性
蜂胶是由蜜蜂收集来自不同的树脂类物质混合物所组成。它含有丰富而独特的黄酮类、芳香酸族脂类、萜烯类等多种有用的物质,以及各种维生素、微量元素、酶还有丰富的有机酸等具有生物活性的成分[1]。为了解蜂胶作为保健食品长期食用的安全性,我们依照《保健食品检验与评价技术规范》(2003年版)于2009年7月对其食用安全性进行评价。
1 材料与方法
1·1 材料 蜂胶软胶囊内容物为棕黄色粘稠状液体,由山东某企业提供,人体推荐量为每日2·0g/60kg·bw。实验时以食用大豆油为溶剂将样品配制成所需浓度供动物试验使用。SPF级昆明种小鼠和Wistar大鼠由北京康蓝生物技术有限公司提供[生产许可证号:SCXK(京)2005-0013]。实验动物使用许可证号:SYXK(鲁)20080005。
1·2 方法[2]
1·2·1 急性毒性试验
选雌雄小鼠各10只,采用最大耐受剂量法,灌胃前16h禁食,自由饮水。第2d以10·0g/kg·bw灌胃,连续观察14h,记录动物中毒症状及死亡情况。
1·2·2 遗传毒性试验
Ames试验:采用平板掺入法,选经鉴定符合要求的鼠伤寒沙门菌组氨酸缺陷型TA97、TA98、TA100、TA102,体外活化系统为多氯联苯诱导的大鼠肝匀浆制备的S-9混合液。试验设立8、40、200、1 0005、000μg/皿5个剂量,同时设立自发回变组、溶剂对照组(丙酮)和阳性对照组。在加S-9与不加S-9混合液的条件下进行,整套试验在相同条件下重复做2次。小鼠骨髓嗜多染红细胞微核试验:选择小鼠50只,随机分为5组,每组10只,雌雄各半。3个实验组染毒剂量分别为2·5、5·0、10·0g/kg·bw,另设食用大豆油阴性对照组和环磷酰胺阳性对照组(40 mg/kg·bw)。灌胃给予实验动物,灌胃量为0·15 ml/10 g·bw,共2次,间隔24 h,末次给予受试物后6 h处死动物,常规制片。每只动物镜检1 000个嗜多染红细胞(PCE),记录微核细胞数,计算微核率(‰)。小鼠精子畸形试验:选择雄性小鼠25只,随机分为5组。每组5只。3个实验组染毒剂量分别为2·5、5·0、10·0g/kg·bw,另设食用大豆油阴性对照组和环磷酰胺阳性对照组(40mg/kg·bw)。灌胃给予实验动物,灌胃量为0·15ml/10g·bw。每天灌胃1次,连续5 d,首次灌胃后第35 d处死动物,常规制片。每只动物计数1000个结构完整的精子,记录畸变类型和数量,计算精子畸形率(%)。
1·2·3 30d喂养试验
选用断乳大鼠80只,随机分为4组,每组20只,雌雄各半。受试物剂量分别为0·83、1·67、3·33g/kg·bw 3个实验组及食用大豆油对照组。每天经口灌胃给与实验动物。各剂量组按照0·5ml/100g·bw灌胃,每日一次,连续30d,自由饮食。每周称体重和食物剩余量、撒食量,计算增重、进食量及食物利用率,实验末期采血进行血常规、血生化测定,解剖动物并取材进行组织病理学检查。
1·2·4 数据处理
使用Microsoft Excel和Stata、Spss软件进行均数、标准差的计算和方差分析或秩和检验,数据以均数±标准差(-x±s)形式表示。
2 结果
2·1 急性毒性试验实验
期间未见明显中毒症状,动物无死亡。最大耐受量试验结果显示,该受试物对两种性别小鼠的MTD均大于10g/kg·bw。根据急性毒性分级标准属实际无毒级物质。
2·2 遗传毒性试验
2·2·1 Ames试验
各剂量组回变菌落数加S-9与不加S-9条件下均未超过自发回变菌落数的2倍,亦无剂量-反应关系,说明Ames试验结果为阴性。
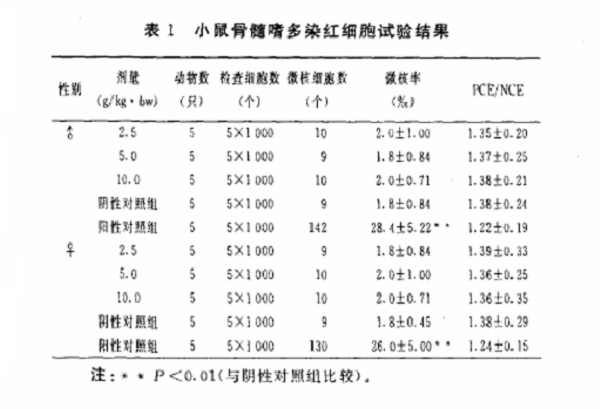
2·2·2小鼠骨髓嗜多染红细胞微核试验
各剂量组微核率与阴性对照组之间差异无统计学意义(P>0·05),而环磷酰胺阳性对照组与阴性对照组之间差异有统计学意义(P<0·01),说明该样品无致小鼠骨髓嗜多染红细胞微核作用。见表1。
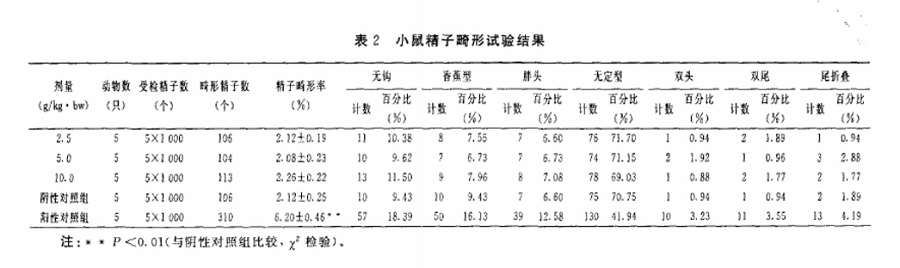
2·2·3 小鼠精子畸形试验
各剂量组小鼠精子畸形率与阴性对照组之间差异无统计学意义(P>0·05),而环磷酰胺阳性对照组与阴性对照组之间差异有统计学意义(P<0·01),说明该样品无致小鼠精子畸形作用。见表2。
2·3 大鼠30 d喂养试验
2·3·1 动物的一般表现
试验周期内各实验组动物总体生长状况良好,体重逐周增长,未见中毒体征及死亡。
2·3·2 体重、食物利用率测定结果
各实验组动物每周体重、进食量、食物利用率和体重增重、总进食量、总食物利用率与对照组之间比较差异无统计学意义(P>0·05)。见表3、表4。


2·3·3 血液学测定结果实验动物雌性高剂量组血红蛋白数、低剂量组白细胞计数与对照组比较差异有统计学意义(P<0·05),但仍在本实验室正常范围内,不认为存在生物学意义。其他各剂量组血液学指标与对照组之间均差异无统计学意义(P>0·05)。见表5。

2·3·4 血液生化学测定结果实验组动物雄性高剂量组尿素氮,雌性高剂量组白/球蛋白比与对照组比较差异有统计学意义(P<0·05),但仍在本实验室正常范围内,不认为存在生物学意义。其他各剂量组血生化指标与对照组之间均差异无统计学意义(P>0·05)。见表6。

2·3·5 病理解剖
2·3·5·1 大体解剖
实验结束时对所有动物进行大体检查,肝脏大小正常、颜色新鲜、表面光滑、质地柔软、边缘锐利、无结节包块等。取出两侧肾和肾上腺,对准肾门将肾以最大剖面剖开,暴露肾盂,检查皮质和髓质的厚度、颜色正常,界限清晰。未见胃肠粘膜出血、溃疡、增厚、淋巴滤泡增生等病变。观察脾切面马氏小体清晰可辨。睾丸/卵巢形态、大小正常。各实验组动物的肝、肾、胃、肠、脾和卵巢/睾丸组织中,未见明显异常。
2·3·5·2 脏器系数测定结果
肝、脾、肾、睾丸等脏器的重量和脏器系数与对照组之间差异均无统计学意义。见表7。

3 讨论
蜂胶的应用十分广泛,具有较强的抗菌消炎、抗病毒、抗肿瘤、增强免疫力、降血糖、保肝护胆的功效,蜂胶长期服用安全无毒,将对开发新药的来源大有前途[3]。为了保证蜂胶软胶囊做为保健食品的食用安全性,我们对该样品进行了急性毒性试验、Ames试验、小鼠骨髓微核试验、小鼠精子畸形试验和大鼠30d喂养试验。在急性毒性试验中,雌雄小鼠最大耐受剂量均大于10g/kg·bw,根据急性毒性分级标准属实际无毒物质。在遗传毒性试验中,Ames试验、小鼠骨髓微核试验、小鼠精子畸形试验3项结果均为阴性,表明在本实验条件下,该受试物未显示有遗传毒性作用。在大鼠30d喂养试验中,各实验组动物生长发育良好,体重增重、食物利用率、脏器系数等各项指标均在本实验室正常值范围内。实验组血常规、血液生化指标均在本实验室值正常范围内。病理组织学检查实验组各脏器未见异常改变。实验结果表明,该样品30d喂养对大鼠各观察指标未产生明显影响。根据以上结果,我们可以初步判断,在推荐量范围内服用本蜂胶软胶囊是安全可靠的。
参考文献:
[1] 黄佳宁,陈秀锦,陈冠敏,等.蜂胶的亚急性毒性研究[J].海峡科学,2009,29⑸:3-7.
[2] 卫生部.保健食品检验与评价技术规范(2003版)[S].177-225.
[3] 关玉.蜂胶的药理实验与临床应用[J].中国实用医药,2009,28,(4):125-126.
- 新渔公众号
- 微信扫一扫
-

- 新渔商城
- 微信扫一扫
-





